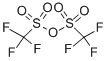
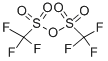
| Περιγραφή |
Ο τριφθορομεθανοσουλφονικός ανυδρίτης, επίσης γνωστός ως τριφλικός ανυδρίτης, έχει αποδειχθεί ότι είναι ένα εξαιρετικό αντιδραστήριο για ένα ευρύ φάσμα μετασχηματισμών. Ως εμπορικά και άμεσα διαθέσιμο αντιδραστήριο, έχει χρησιμοποιηθεί ευρέως στη συνθετική χημεία λόγω της υψηλής ηλεκτροφιλικότητας του. Δεδομένης της υψηλής συγγένειάς του προς τα Ο-πυρηνόφιλα, ευνοείται έντονα η αντίδραση με αλκοόλες, καρβονύλια, οξείδια του φωσφόρου του θείου και του ιωδίου προς το σχηματισμό των αντίστοιχων τριφλικών. Ως μία από τις κορυφαίες αποχωρούσες ομάδες στην οργανική χημεία, τα παραγόμενα τριφίδια ανοίγουν στη συνέχεια την πόρτα σε διάφορους μετασχηματισμούς κατάντη, συμπεριλαμβανομένων (αλλά δεν περιορίζονται σε) αντιδράσεις υποκατάστασης, διεργασίες διασταυρούμενης σύζευξης, αντιδράσεις οξειδοαναγωγής και αναδιατάξεις[1-2] . |
| Χημικές ιδιότητες |
διαυγές άχρωμο έως ανοιχτό καφέ υγρό |
| Χρήσεις |
Ο τριφθορομεθανοσουλφονικός ανυδρίτης είναι ένα ισχυρό ηλεκτρόφιλο που χρησιμοποιείται στη χημική σύνθεση για την εισαγωγή της τριφλυλικής ομάδας. |
| Χρήσεις |
Ο τριφθορομεθανοσουλφονικός ανυδρίτης χρησιμοποιείται για τη μετατροπή των φαινολών και της ιμίνης σε τριφλικό εστέρα και ομάδα NTf. Είναι ένα ισχυρό ηλεκτρόφιλο που χρησιμοποιείται για την εισαγωγή της τριφλυλικής ομάδας στη χημική σύνθεση. Χρησιμεύει ως αντιδραστήριο στην παρασκευή τριφλικών αλκυλίου και βινυλίου και για τη στερεοεκλεκτική σύνθεση δοτών μεθυλουρονικού μαννοσαζίδης. Λειτουργεί ως καταλύτης για γλυκοζυλίωση με ανωμερή υδροξυσάκχαρα για την παρασκευή πολυσακχαριτών. |
| Ορισμός |
ChEBI: Ο τριφλικός ανυδρίτης είναι ένας οργανοσουλφονικός ανυδρίτης. Σχετίζεται λειτουργικά με ένα τριφλικό οξύ. |
| Προφίλ αντιδραστικότητας |
Η ηλεκτροφιλική ενεργοποίηση τριτογενών και δευτεροταγών αμιδίων με τριφλικό ανυδρίτη (Tf2O, ριφθορομεθανοσουλφονικός ανυδρίτης) υπό ήπιες συνθήκες δημιουργεί τριφλικά ιμίνιο και ιμινο, αντίστοιχα, τα οποία θα μπορούσαν να χρησιμοποιηθούν ως ευέλικτα αντιδραστήρια για να αντιδράσουν με διάφορα C-, N-, O- και S. -πυρηνόφιλα για τη μετατροπή μιας αμιδικής λειτουργίας σε διαφορετικά προϊόντα. Άλλα πυρηνόφιλα που περιέχουν οξυγόνο, όπως τα σουλφοξείδια και τα οξείδια του φωσφόρου, θα μπορούσαν επίσης να υποστούν πυρηνόφιλη επίθεση με Tf2O για να δημιουργήσουν τριφλικό θειονίου, ηλεκτροφιλικά είδη P και τριφλικό φωσφόνιο. Αυτά τα εξαιρετικά ενεργά παροδικά είδη θα μπορούσαν εύκολα να υποστούν πυρηνόφιλες αντιδράσεις υποκατάστασης για περαιτέρω διαφορετικούς μετασχηματισμούς. Επιπλέον, λόγω της ισχυρής ηλεκτροφιλικής ιδιότητας, το Tf2O είναι επιρρεπές να αντιδρά με σχετικά ασθενή πυρηνόφιλα, όπως ομάδες νιτριλίου ή ορισμένες ετεροκυκλικές ενώσεις που περιέχουν άζωτο. Επιπλέον, το Tf2O έχει επίσης χρησιμοποιηθεί ως αποτελεσματικό αντιδραστήριο ριζικής τριφθορομεθυλίωσης και τριφθορομεθυλθειολίωσης μέσω της απελευθέρωσης SO2 ή διαδικασίας αποοξυγόνωσης για τη σύνθεση τριφθορομεθυλιωμένων και τριφθορομεθυλθειολωμένων ενώσεων[2]. |
| Κίνδυνος |
Μπορεί να είναι διαβρωτικό για τα μέταλλα. Επιβλαβές σε περίπτωση κατάποσης. Προκαλεί σοβαρά δερματικά εγκαύματα και βλάβες στα μάτια. |
| Αναφλεξιμότητα και Εκρηκτικότητα |
Μη ταξινομημένο |
| Σύνθεση |
Η σύνθεση του τριφθορομεθανοσουλφονικού ανυδρίτη έχει ως εξής:
Μια ξηρή φιάλη {{0}}ml με στρογγυλό πάτο γεμίζεται με 36,3 g. (0.242 mole) τριφθορομεθανοσουλφονικού οξέος (Σημείωση 1) και 27,3 g. (0,192 mole) πεντοξειδίου του φωσφόρου (Σημείωση 2). Η φιάλη πωματίζεται και αφήνεται να παραμείνει σε θερμοκρασία δωματίου για τουλάχιστον 3 ώρες. Κατά τη διάρκεια αυτής της περιόδου το μίγμα της αντίδρασης μεταβάλλεται από πολτό σε στερεή μάζα. Η φιάλη είναι εφοδιασμένη με κεφαλή απόσταξης μικρής διαδρομής και θερμαίνεται πρώτα με ένα ρεύμα θερμού αέρα από ένα πιστόλι θερμότητας και στη συνέχεια με τη φλόγα από έναν μικρό καυστήρα.Η φιάλη θερμαίνεται μέχρι να σταματήσει η απόσταξη τριφθορομεθανοσουλφονικού ανυδρίτη, bp 82–115 βαθμούς, δίνοντας 28,4–31,2 g. (83–91%) του ανυδρίτη, ένα άχρωμο υγρό. Αν και αυτό το προϊόν είναι επαρκώς καθαρό για χρήση στο επόμενο στάδιο, το υπόλοιπο οξύ μπορεί να αφαιρεθεί από τον ανυδρίτη με την ακόλουθη διαδικασία. Ένας πολτός 3,2 γρ. πεντοξειδίου του φωσφόρου σε 31,2 γρ. του ακατέργαστου ανυδρίτη αναδεύεται σε θερμοκρασία δωματίου σε πωματισμένη φιάλη για 18 ώρες. Αφού τοποθετηθεί στη φιάλη αντίδρασης μια κεφαλή απόσταξης μικρής διαδρομής, θερμαίνεται με ελαιόλουτρο, αποδίδοντας 0.7 g. του προδρόμου, bp 74–81 μοίρες, ακολουθούμενη από 27,9 g. του καθαρού ανυδρίτη τριφθορομεθανοσουλφονικού οξέος, bp 81–84 βαθμοί.

|
| αποθήκευση |
Φυλάσσεται σε δροσερό, ξηρό, καλά αεριζόμενο χώρο. Ευαίσθητο στην υγρασία. |
| Μέθοδοι Καθαρισμού |
Μπορεί να παρασκευαστεί πρόσφατα από το άνυδρο οξύ (11,5 g) και το P2O5 (11,5 g, ή το μισό από αυτό το βάρος) αφήνοντας στην άκρη σε θερμοκρασία δωματίου για 1 ώρα, αποστάζοντας τα πτητικά προϊόντα και στη συνέχεια αποστάζεται μέσω μιας κοντής στήλης Vigreux. Υδρολύεται εύκολα από το H2O και αποσυντίθεται αισθητά μετά από μερικές ημέρες για να απελευθερώσει SO2 και να παράγει ένα παχύρρευστο υγρό. Αποθηκεύστε το στεγνό σε χαμηλές θερμοκρασίες. [Burdon et al. J Chem Soc 2574 1957, Beard et al. J Org Chem 38 373 1973, Beilstein 3 IV 35.] |
| βιβλιογραφικές αναφορές |
[1] Haoqi Zhang. "Τριφθορομεθανοσουλφονικός ανυδρίτης σε ενεργοποίηση αμιδίου: ένα ισχυρό εργαλείο για τη δημιουργία ετεροκυκλικών πυρήνων." TCIMAIL (2021).
[2] Δρ. Qixue Qin, Καθ. Dr. Ning Jiao, Zengrui Cheng. "Πρόσφατες εφαρμογές του τριφθορομεθανοσουλφονικού ανυδρίτη στην οργανική σύνθεση." Angewandte Chemie 135 10 (2022). |